-
2021 소방간부 화학개론 (11번 ~ 15번 )소방공무원/화학개론 2021. 12. 5. 14:10728x90반응형
11. [표]는 금속 A, B, C의 산화-환원 반응성을 비교한 실험 결과이다

이에 대한 설명으로 옳지 않은 것은? (단, A, B, C는 임의의 원소이고, 수용액의 금속이온은 모두 +2가 상태이며 물은 반응하지 않는다.)
① 실험 (가)에서는 수용액에 A2+ 이온이 생성된다.
② 원자량은 B가 C보다 크다.
③ A, B, C 중 산화 경향성이 가장 큰 것은 A이다.
④ B 금속판을 A2+ 수용액에 담그면 금속판의 질량이 감소한다.
⑤ C 금속판을 A2+ 수용액에 담그면 금속판의 질량이 변하지 않는다.
답: 4번
풀이
(가) A의 금속판의 질량이 변화되었으니 B가 환원된 것이다
-> 산화경향성: A > B , 원자량: A < B
(나) B의 금속판의 질량이 감소되었으니 B가 산화된 것이다
-> 산화경향성: B > C , 원자량: B > C
반응성: A > B > C
④ B 금속판을 A2+ 수용액에 담그면 산화경향성이 A가 강하기 때문에 금속판의 질량은 변하지 않는다
12. [그림]은 일정한 양의 고체 X에 열을 가해 액체를 거쳐 기체로 변화시키는 과정의 온도 변화를 나타낸 것이다

답: 3/4
풀이
Q = cmΔT = CΔT
Q1 = cm x 60 = 1 -> c1 = 1/60
Q2 = cm x 90 = 2 -> c2 = 2/90
c1 / c2 = 1/60 / 2/90 = 3/4
13. 다음은 하이드라진(N2H4)의 연소반응을 열화학 반응식으로 나타낸 것이다.

이 반응에서 계의 엔트로피변화(ΔS계), 주위의 엔트로피변화(ΔS주위), 전체 엔트로피변화(ΔS전체)와 반응의 자발성을 옳게 나타낸 것은?

답: 1번
풀이
ΔS계 + ΔS주위 = ΔS우주
ΔS계 > 0 (반응물의 기체몰수 < 생성물의 기체몰수)
ΔS주위 > 0 (발열반응)
ΔG = ΔH - TΔS < 0 -> 자발적
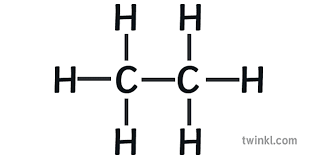
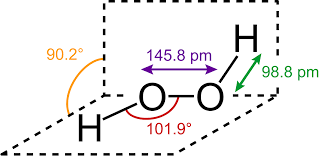
14. 다음은 세 가지 분자의 분자식을 나타낸 것이다.

이에 대한 설명으로 옳은 것은?
① 분자의 극성이 가장 큰 것은 (가)이다.
② 끓는점은 (가)가 (나)보다 높다.
③ 공유 전자쌍의 수는 (다)가 가장 많다.
④ (다)의 분자 모양은 선형 구조이다.
⑤ 결합각은 (가)의 H-C-H가 (나)의 H-N-H보다 크다
답: 5번
풀이
① 분자의 극성이 가장 작은 것은 (가) 이다.
② 끓는점은 (가)가 (나)보다 낮다.
③ 공유 전자쌍의 수는 (나)가 가장 많다.
④ (다)의 분자 모양은 굽은형 구조이다.

15. 수소 원자에서 n(주양자수) = 1의 바닥상태에 있던 전자가 n =3의 들뜬상태가 되었다. 이에 대한 다음 설명에서 옳은 것은?
① 바닥상태보다 n = 3인 상태의 전자를 이온화(완전히 제거)하는데 더 많은 에너지가 필요하다.
② n = 1인 상태의 전자보다 n = 3인 상태의 전자가 평 균적으로 핵으로부터 멀리 떨어져 있다.
③ n = 3인 상태는 첫 번째 들뜬상태이다.
④ 전자가 n = 3인 상태에서 n = 2인 상태로 전이될 때 방출하는 빛의 파장은, n = 3인 상태에서 n = 1인 상태로 전이될 때보다 짧다.
⑤ 전자가 n = 3인 상태에서 바닥상태로 전이될 때 방출하는 빛의 파장은, 바닥상태에서 n = 2인 상태로 전이될 때 흡수하는 빛의 파장과 같다.
답: 2번
풀이
① 에너지 준위가 바닥상태일때보다 들뜬 상태에서가 높기 때문에 들뜬상태에서 제거하는 에너지가 적게 든다
③ n = 3인 상태는 첫 번째 들뜬상태는 아니다.
④ 전자가 n = 3인 상태에서 n = 2인 상태로 전이될 때 방출하는 빛의 파장은 가시광선이고 n = 3인 상태에서 n = 1인 상태로 전이될 때 방출되는 빛의 파장은 자외선이다. 빛의 파장은 가시광선 > 자외선
⑤ 전자가 n = 3인 상태에서 바닥상태로 전이될 때 방출하는 빛의 파장은, 바닥상태에서 n = 2인 상태로 전이될 때 흡수하는 빛의 파장보다 짧다
728x90반응형'소방공무원 > 화학개론' 카테고리의 다른 글
2021 소방간부 화학개론 (21번 ~ 25번) (3) 2021.12.05 2021 소방간부 화학개론 (16번 ~ 20번) (0) 2021.12.05 2021 소방간부 화학개론 (6번~10번) (0) 2021.12.05 2021 소방간부 화학개론 (1번 ~ 5번) (0) 2021.12.05 2020 소방간부 화학개론 (21번 ~ 25번) (0) 2021.12.04
