-
2020 소방간부 화학개론 (21번 ~ 25번)소방공무원/화학개론 2021. 12. 4. 17:47728x90반응형
21. 수소 연료 전지에서 일어나는 반응이다.
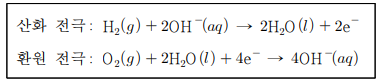
TK, P기압에서 H2(g) 10VL가 소모되었을 때, 전체 반응에서 생성되는 H2O(l)의 질량(g)은? (단, TK, P기압에서 수소(H2) 기체 1몰의 부피는 VL 이고, H2O의 분자량은 18 g /mol이다.)
답: 180g
풀이:
2H2 + 4OH- -> 4H2O + 4e-
O2 + 2H2O + 4e- -> 4OH-
=> 2H2 + O2 -> 2H2O
10몰 10몰
1몰: x몰 = VL : 10VL -> x몰 = 10몰
몰 = 질량 / 분자량
질량 = 몰 x 분자량 = 10mol x 18g/mol = 180g
22. 탄소(C)를 포함한 4가지 물질의 분자식이다.

4가지 물질에 포함된 탄소(C)의 산화수를 모두 더한 값은?
답: 0
풀이:
CO2 의 C의 산화수 = +4
HCN의 C의 산화수 = +2
CH4의 C의 산화수 = -4
CH3Cl의 C의 산화수 = -2
< HCN의 산화수 >

- HCN 에선 C이 H와 단일결합 N삼중결합을 하고 있다.
- 전기음성도가 강한 질소가 탄소의 전자 3개를 끌어당겨 질소의 산화수는 -3이다
- 탄소는 수소의 전자 1개를 끌어당겨 수소의 산화수는 +1이다.
- HCN의 산화수 총합은 0이므로 탄소의 탄화수는 +2이다
< 산화수 >
- 전기음성도에 의해 전자를 끌어당기는 수만큼 -1 x n
- 전기음성도에 의해 전자를 뺏기는 수만큼 +1 x n
23. 다음 열화학 반응식에 대한 설명으로 옳은 것은? (단, C, O의 원자량은 각각 12, 16이고, ∆H°는 25 ℃ 에서의 표준 반응열이다.)

① 이 반응은 흡열 반응이다.
② 생성물보다 반응물이 더 안정하다.
③ CO(g)의 표준 연소열은 -566 kJ /mol이다.
④ CO2(g)의 표준 생성열은 -283 kJ /mol이다.
⑤ CO2(g) 7 g이 연소할 때는 70.75 kJ의 열이 방출된다
답: 5번
풀이
ΔH˚ > 0 흡열반응 , ΔH˚ < 0 발열반응
ΔS˚ < 0
ΔG˚ = ΔH˚ - TΔS˚ < 0
① 이 반응은 발열 반응이다.
② 생성물보다 반응물이 덜 안정하다.
③ CO(g)의 표준 연소열은 -283 kJ /mol이다.
④ CO2(g)의 표준 생성열은 C(s) + O2(g) -> CO2(g) 때 발생되는 열이다
⑤ CO2(g) 7 g이 연소할 때는 70.75 kJ의 열이 방출된다
24. 금속 X와 Y의 단위 세포에 대한 자료이다.

빈칸에 들어갈 내용으로 옳은 것은?
답: ㄱ : 4 , ㄴ: 체심
풀이
(가) 면심입방구조 (나) 체심입방구조
< 고체결정구조 >

1. 단순입방구조
- 쌓임형태 : a - a - a - a
- 배위수 = 6
- 단위세포당 입자수 = 1
- 공간점유율 = 52%
2. 체심입방구조
- 쌓임형태 : a - b - a - b
- 배위수 = 8
- 단위세포당 입자수 = 2
- 공간점유율 = 68%
3. 면심입방구조
- 쌓임형태 : a - b - c - a - b - c
- 배위수 = 12
- 단위세포당 입자수 = 4
- 공간점유율 = 74%
25. 그림은 콕으로 연결한 두 플라스크에 각각 질소 (N2) 기체와 산소(O2) 기체를 넣은 것이다. 일정한 온도에서 콕을 열고 평형에 도달하였을 때, 전체 압력 (atm)은? (단, N2와 O2는 이상기체이고, 서로 반응하지 않는다.)

답: 4/3
풀이
PV = nRT
n = PV/RT
N2의 몰수 = 4/RT , O2의 몰수 = 4/RT
콕을 열었을때 총 부피 6L, 기체의 몰수 8/RT
P = n/V RT ∝ 8/RT ÷ 6 = 4/3
728x90반응형'소방공무원 > 화학개론' 카테고리의 다른 글
2021 소방간부 화학개론 (6번~10번) (0) 2021.12.05 2021 소방간부 화학개론 (1번 ~ 5번) (0) 2021.12.05 2020 소방간부 화학개론 (16번 ~ 20번) (0) 2021.12.04 2020 소방간부 화학개론 (11번 ~ 15번) (0) 2021.12.04 2020 소방간부 화학개론 (6번 ~ 10번) (1) 2021.12.04