-
2019 소방간부 화학개론 (21번 ~ 25번)소방공무원/화학개론 2021. 12. 3. 20:04728x90반응형
21. C, H, O로 구성된 화합물 X 23 mg을 완전 연소 시켰더니 CO2 44mg과 H2O 27mg이 생성되었다. X의 실험식은? (단, H, C, O의 원자량은 각각 1, 12, 16이다.)

답: 5번
풀이
C2H6O1 + 3O2 -> 2CO2 + 3H2O
0.5mol 1mol 1.5mol
22. 표는 3가지 고체 결정 구조의 단위 세포에 들어 있는 입자 수와 가장 인접한 입자수를 나타낸 것이다. ㄱ∼ㄷ으로 옳은 것은?
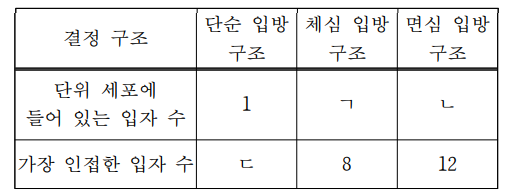
답: ㄱ-2 , ㄴ-4 , ㄷ-6
< 고체결정구조 >

1. 단순입방구조
- 쌓임형태 : a - a - a - a
- 배위수 = 6
- 단위세포당 입자수 = 1
- 공간점유율 = 52%
2. 체심입방구조
- 쌓임형태 : a - b - a - b
- 배위수 = 8
- 단위세포당 입자수 = 2
- 공간점유율 = 68%
3. 면심입방구조
- 쌓임형태 : a - b - c - a - b - c
- 배위수 = 12
- 단위세포당 입자수 = 4
- 공간점유율 = 74%
23. 0.5M 포름산(HCOOH, Ka= 2.0 x 10^-4 ) 수용액의 pH는?

답: 2
풀이
pH = pKa + log[A-]/[HA] 로 푸는 것이 아님
포름산은 약산이고 포름산의 농도만 제시되어 있기 때문에 이온화도를 알아야 한다
α = √(Ka/C) -> pH= -log√(KaC) = -log( 2 x 10^-4 x 0.5 ) = 2
24. 25℃에서 10.0 % NaOH 수용액의 밀도가 1.10g/mL일 때, 이 수용액의 몰농도(M)는? (단, NaOH의 화학식량은 40.0이다.)
답: 2.75 M
풀이
10% NaOH 수용액 100 g 있다고 가정하고 10 g NaOH + 90 g H2O으로 둔다
NaOH mol수 = 10 g / (40 g/mol) = 0.25 mol
수용액 부피 = 100 g / (1.10 g/mL) = 1000/11 mL
몰농도 = 용질 mol수 / 용액 L수
= 0.25 mol / 1/11 L = 2.75 M
25. 밀폐된 강철 용기에 에테인(C2H6 ) 30 g과 산소(O2 ) 160 g을 넣고 완전 연소 반응을 완결시켰을 때, 강철 용기에 존재하는 물질의 총 몰수는? (단, H, C, O의 원자량은 각각 1, 12, 16이다.)
답: 6.5mol
풀이 :
2C2H6 + 7O2 -> 4CO2 + 6H2O
1mol 5mol
-1mol -3.5mol 2mol 3mol
강철용기에 존재하는 물질 : O2 1.5mol, CO2 2mol, H2O 3mol
총 6.5mol
728x90반응형'소방공무원 > 화학개론' 카테고리의 다른 글
2020 소방간부 화학개론 (6번 ~ 10번) (1) 2021.12.04 2020 소방간부 화학개론 (1번 ~ 5번) (0) 2021.12.04 2019 소방간부 화학개론 (16번 ~ 20번) (0) 2021.12.03 2019 소방간부 화학개론 (11번 ~ 16번) (0) 2021.12.03 2019 소방간부 화학개론 (6번 ~ 10번) (0) 2021.12.03